EAU 2025:mCRPC 决策制定算法
EAU 2025:mCRPC 决策制定算法
摘要
Christopher Sweeney 博士在 2025 年 EAU 年会上介绍了针对 mCRPC 的个体化治疗决策算法,该算法基于生物标志物检测结果,为患者提供最优的一线治疗方案。算法包括 LuPSMA 放射性配体疗法、PARP 抑制剂和化疗组合等,并强调了生物标志物阴性患者的治疗选择。
概述
Christopher Sweeney 博士在 2025 年欧洲泌尿外科协会 (EAU) 年会上介绍了针对转移性去势抵抗性前列腺癌 (mCRPC) 的个体化治疗决策算法。该算法基于生物标志物检测结果,为患者提供最优的一线治疗方案选择。
亮点
- 🔬 个性化治疗:mCRPC 一线治疗需根据生物标志物检测结果制定个体化方案
- 🧬 生物标志物指导:PTEN、RB 1、p 53、BRCA 1/2 等基因突变影响治疗选择
- ☢️ LuPSMA 放射性配体治疗:SUVmean>10 的患者中位总生存期达 21 个月
- 💊 PARP 抑制剂:对 BRCA 2、BRCA 1、CDK 12 和 PALB 2 突变患者效果显著
- 🩸 治疗毒性:TALAPRO-2 试验中 PARP 抑制剂输血率高达 42%
- ⚗️ 联合治疗:卡巴他赛+卡铂对 PTEN、RB、p 53 缺失的间变性 mCRPC 患者有效
- 🏥 生物标志物阴性患者:推荐镭-223+恩杂鲁胺或恩杂鲁胺+LuPSMA 方案
- 🔄 治疗顺序:RAPSON 试验比较镭-223 与多西他赛的先后使用顺序
- ❌ 不推荐方案:算法中不包含阿比特龙或'amide 类药物的序贯使用
- 🎯 治疗原则:最大获益来自一线治疗,许多患者无法进入下一线治疗
配图
根据提供的文章内容,我将结合配图对 mCRPC(转移性去势抵抗性前列腺癌)的决策算法进行结构化解析:
一、核心治疗框架
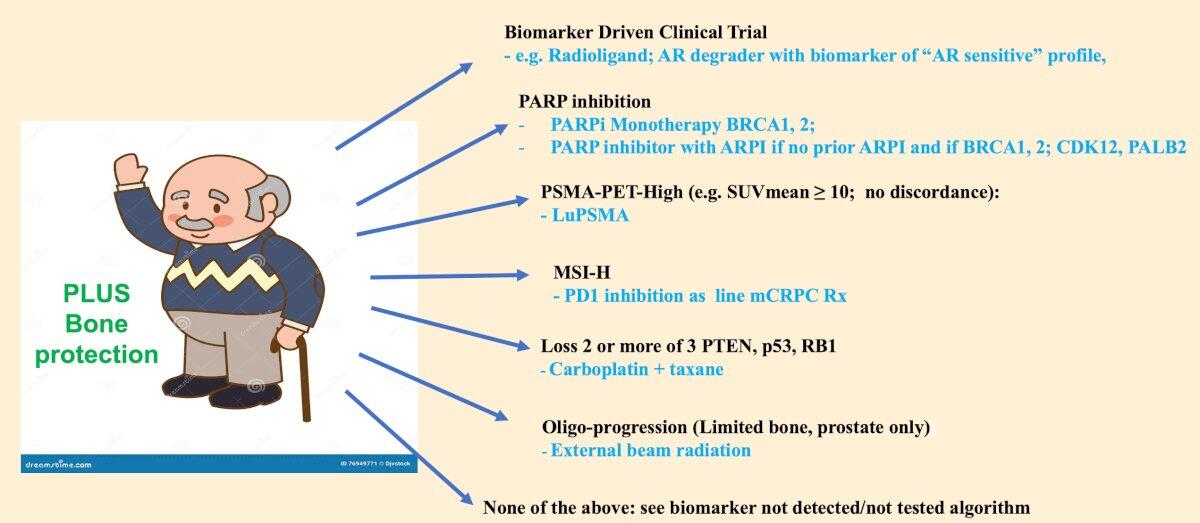
关键逻辑链:
- 生物标志物检测先行:必须检测 PTEN/RB 1/p 53/BRCA 等基因突变及 PSMA PET(SUVmean 值)
- 阳性患者→匹配靶向治疗(如 PARPi 对应 DDR 突变)
- 阴性/未知患者→选择非靶向方案(如镭-223 联合治疗)
二、关键治疗模块详解
1. LuPSMA 放射性配体疗法
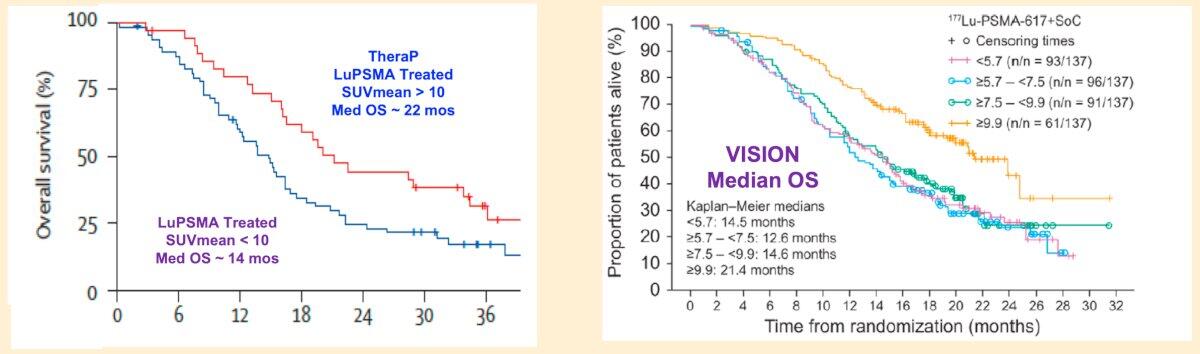
- 筛选标准:PSMA PET 的 SUVmean 阈值(>10 vs <10)
- 生存差异:
- SUVmean>10:中位 OS 21 个月(vs 15 个月对照组)
- SUVmean<10:仅延长 2 个月(14 vs 12 个月)→ 70%患者可能获益有限
- 临床启示:避免因无效治疗延误后续 PARPi 等更有效方案
2. PARP 抑制剂精准应用
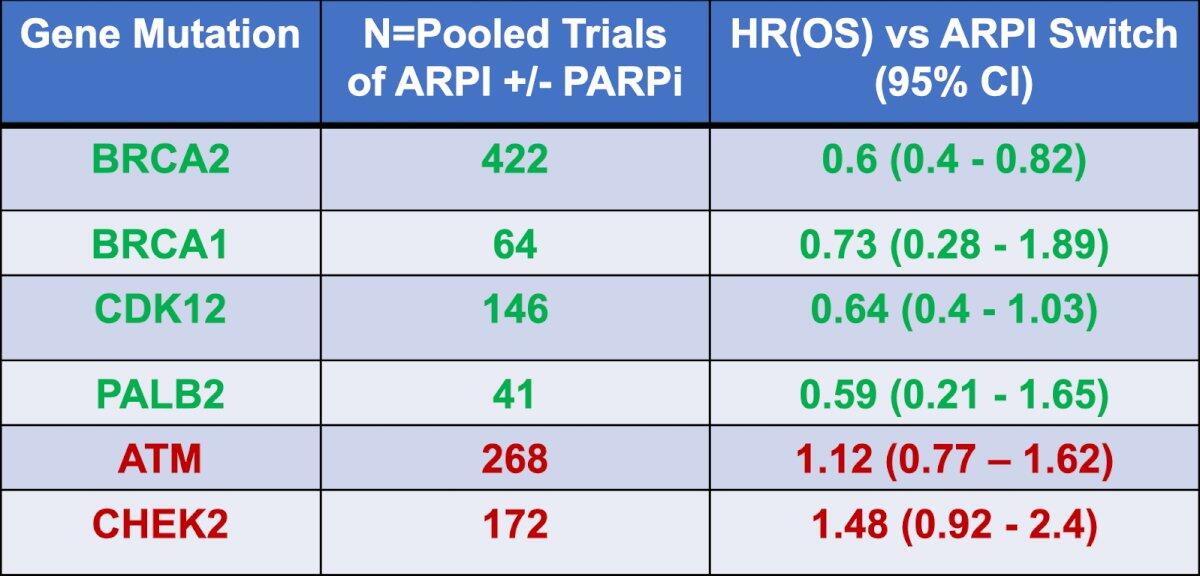
- 显著获益突变:BRCA 2 > BRCA 1 > CDK 12/PALB 2
- 有限获益突变:ATM/CHEK 2(不推荐优先使用)
- 毒性警示:TALAPRO-2 试验中 42%需输血
3. 化疗组合的分子选择
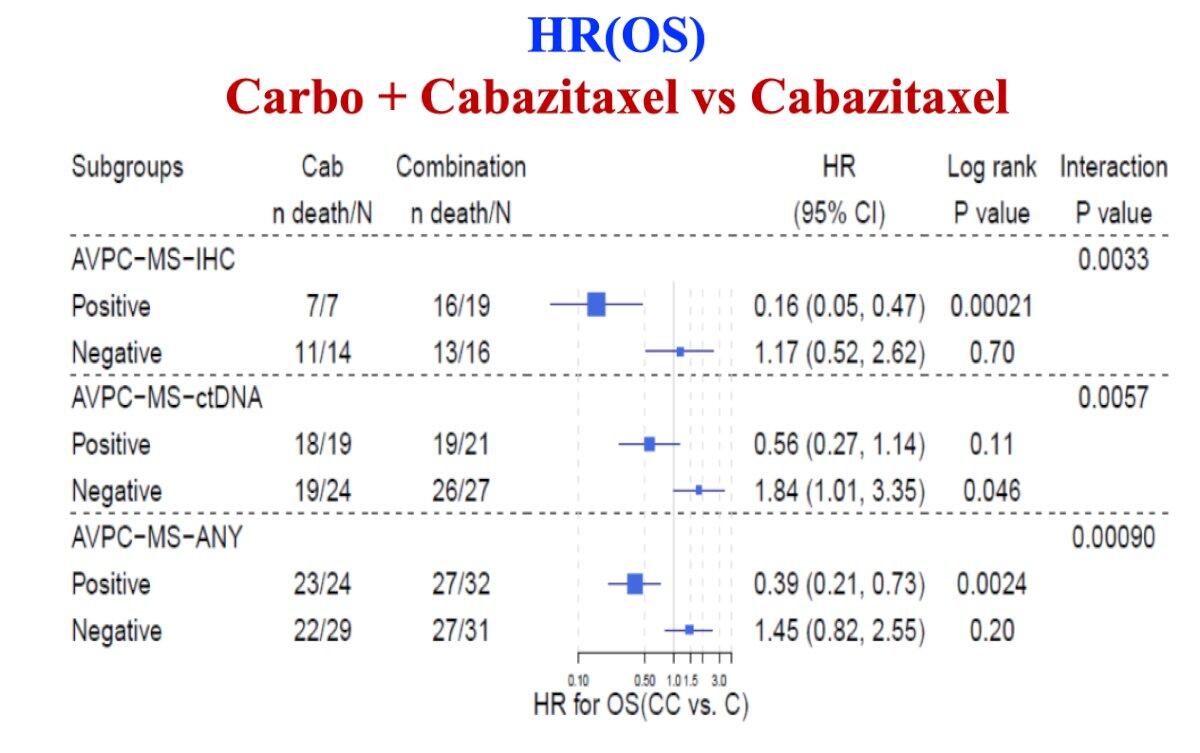
- 最佳人群:PTEN/RB/p 53 中缺失≥2 个(间变性特征)
- PFS 提升:4.5→7.3 个月(HR 0.69, p=0.018)
4. 生物标志物阴性患者的选项 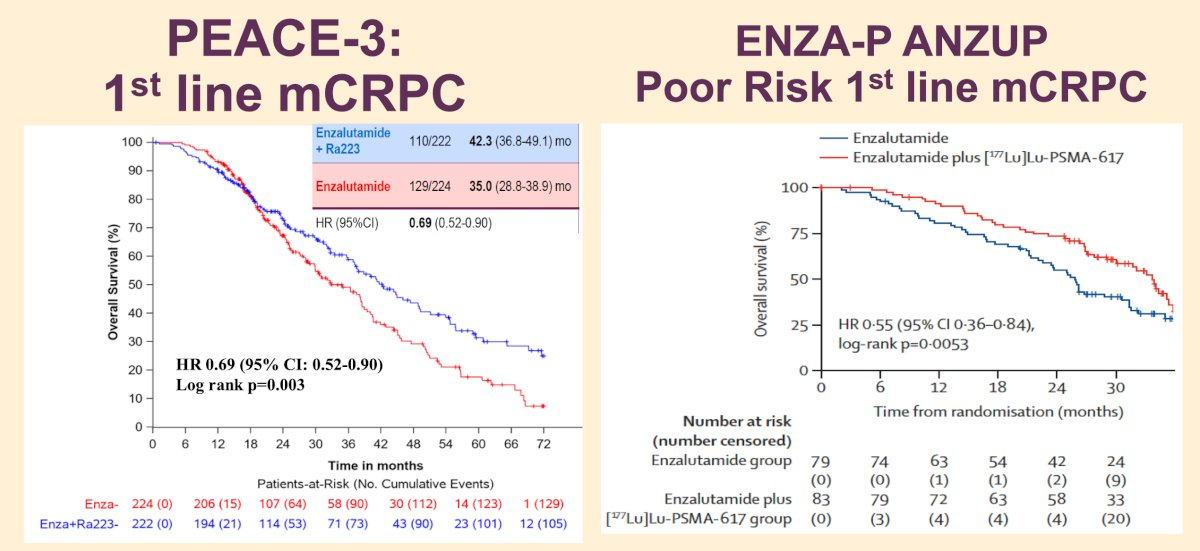
- 镭-223+恩杂鲁胺(基于 PEACE-3 数据)
- 恩杂鲁胺+LuPSMA(ENZA-p 试验)
三、争议与边界
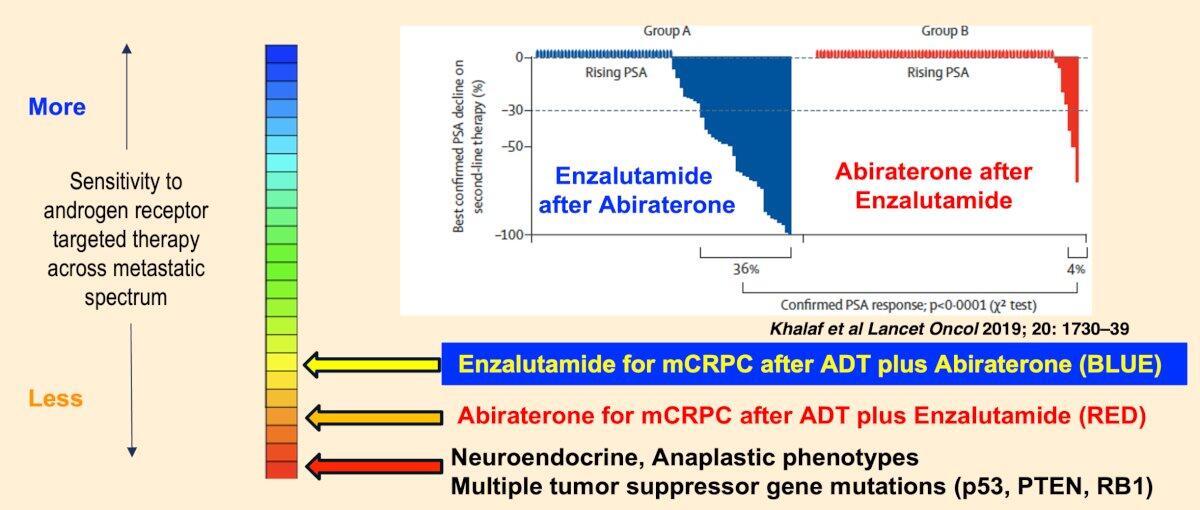
- 明确排除:阿比特龙/恩杂鲁胺序贯使用
- 证据:ADT 单药后 HR 仅 0.7-0.8,中位 OS 约 3 年
- 本质:AR 依赖性在治疗后可能发生根本改变
四、临床实践启示
- 诊断时必检:
- 组织/液体活检(BRCA 等 DDR 基因)
- PSMA PET(筛选 LuPSMA 候选者)
- 治疗排序原则:
%%{init: {'theme':'dark'}}%% graph LR A[生物标志物检测] --> B{阳性?} B -->|是| C[靶向治疗优先] B -->|否| D[镭-223/LuPSMA/化疗组合] - 警惕过度治疗:
- SUVmean<10 者慎用 LuPSMA
- ATM/CHEK 2 突变者避免 PARPi
五、未解问题
- RAPSON 试验中镭-223 与多西他赛序贯的最终生存差异(目前仅 14 例完成交叉)
- PARPi 进展后治疗方案的最佳选择
相关问题
1. 哪些生物标志物对 mCRPC 治疗决策最重要?
- BRCA 1/2、CDK 12 和 PALB 2 突变对 PARP 抑制剂治疗反应最佳
- PTEN、RB 1 和 p 53 缺失提示可能对卡巴他赛+卡铂方案有更好反应
- PSMA PET 显像中 SUVmean>10 预示 LuPSMA 治疗可能获得更好效果
- MMRd 突变患者可考虑 PD 1 抑制剂治疗
2. 为什么 70%的 LuPSMA 治疗患者可能获益有限?
- 这些患者 SUVmean<10,中位总生存期仅比对照组延长 2 个月 (14 vs 12 个月)
- 可能错过更有效的治疗选择 (如 BRCA 突变患者的 PARP 抑制剂)
- 疾病进展后由于临床状态恶化可能失去接受后续治疗的机会
3. PARP 抑制剂的主要局限性是什么?
- 仅对特定 DNA 损伤修复基因突变患者有效
- 毒性较高,TALAPRO-2 试验中输血率高达 42%
- 对 ATM 和 CHEK 2 突变患者效果有限
- 进展后使用 PARP 抑制剂的疗效数据尚不明确
4. 卡巴他赛+卡铂对哪类患者特别有效?
- 具有"间变性 mCRPC 分子特征"的患者
- 即同时缺失 PTEN、RB 和 p 53 三个基因中至少两个的患者
- 该组合将无进展生存期从 4.5 个月延长至 7.3 个月 (HR 0.69)
5. 为什么 Sweeney 博士不推荐阿比特龙或'amide 类药物的序贯使用?
- 这些方案在 ADT 单药治疗后的总生存 HR 仅为 0.70-0.80
- 中位总生存期约 3 年,效果有限
- 在 ADT+AR 通路抑制剂治疗后,肿瘤对 AR 的依赖性存在很大变异
- 实际疗效数据不如其他新型治疗方案显著
link to original note: EAU 2025 My Algorithm for Decision Making in mCRPC